Орган инспекции
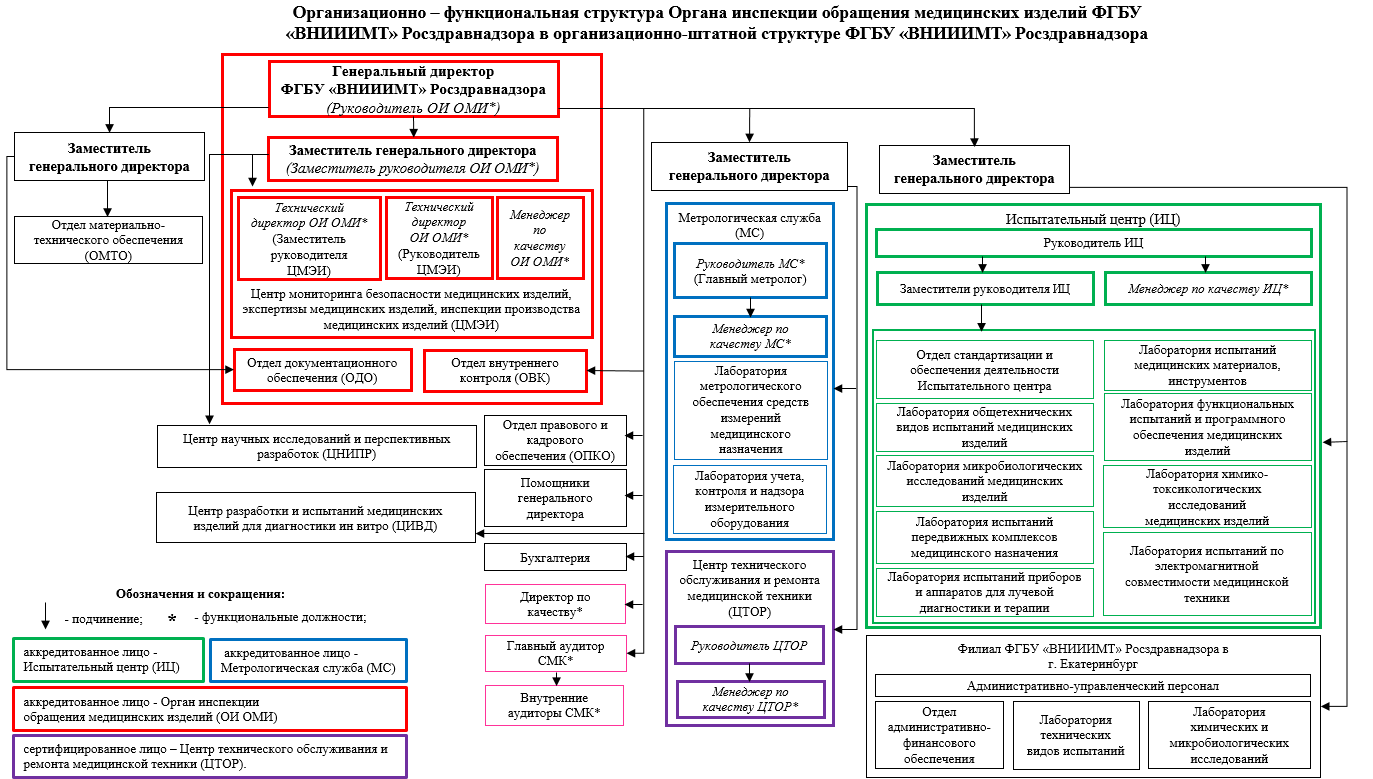
Состав органов управления органа инспекции обращения медицинских изделий
- Руководитель - генеральный директор Иванов Игорь Владимирович
- Заместитель руководителя - заместитель генерального директора Фомина Наталья Михайловна
- Менеджер по качеству - эксперт центра мониторинга безопасности медицинских изделий, экспертизы медицинских изделий, инспекции производства медицинских изделий Дементьев Андрей Николаевич
- Технический директор - руководитель центра мониторинга безопасности медицинских изделий, экспертизы медицинских изделий, инспекции производства медицинских изделий Сапунова Анна Владимировна
- Технический директор - заместитель руководителя центра мониторинга безопасности медицинских изделий, экспертизы медицинских изделий, инспекции производства медицинских изделий Федоров Иван Сергеевич
Примерная стоимость выполнения органом инспекции работ по проведению инспекции производства
Перечень документов
- Заявка на имя Генерального директора ФГБУ "ВНИИИМТ" Росздравнадзора;
- Копия технического задания электронного аукциона;
- Опись документов, прилагаемых к заявке (справка о медицинском изделии, копия регистрационного удостоверения, копия декларации о соответствии или сертификата соответствия (при необходимости), копия технического задания (при наличии), копия эксплуатационных документов).
Все копии должны быть заверены печатью заявителя. Все, что в составе имеет больше 2-х страниц – должно быть прошито и скреплено печатью.
Перечень документов
- Заявка на имя Генерального директора ФГБУ "ВНИИИМТ" Росздравнадзора;
- Определение суда (или постановление следственного комитета), где ФГБУ "ВНИИИМТ" Росздравнадзора указан в качестве экспертной организации (при наличии);
- При отсутствии определения (постановления) необходимо в заявке указать, в рамках какого дела необходима экспертиза;
- Опись документов, прилагаемых к заявке (справка о медицинском изделии, копия регистрационного удостоверения, копия декларации о соответствии или сертификата соответствия (при необходимости), копия технического задания (при наличии), копия эксплуатационных документов).
Все копии должны быть заверены печатью заявителя. Все, что в составе имеет больше 2-х страниц – должно быть прошито и скреплено печатью.
«ФГБУ «ВНИИИМТ» Росздравнадзора осуществляет инспекционные проверки в соответствии с Требованиями к внедрению, поддержанию и оценке системы менеджмента качества медицинских изделий в зависимости от потенциального риска их применения, утвержденными Решением Совета Евразийской экономической комиссии от 10 ноября 2017 г. № 106, и Требованиями к внедрению, поддержанию и оценке системы управления качества медицинских изделий в зависимости от потенциального риска их применения, утвержденными постановлением Правительства российской Федерации от 9 февраля 2022 г. № 136.
Этапы инспекции
- Прием и рассмотрение документов, являющихся основанием для проведения инспекции.
- Первичная оценка документации, представленной для проведения инспекции.
- Анализ представленных материалов и проведение (при необходимости) технических испытаний и токсикологических исследований силами Испытательного центра ФГБУ "ВНИИИМТ" Росздравнадзора.
- Оформление результатов инспекции.
- Взаимодействие с Заявителем.
Работы, выполняемые в рамках проведения контроля за обращением медицинских изделий Федеральной службой по надзору в сфере здравоохранения (Росздравнадзором), выполняются на основании государственного задания и финансируются Росздравнадзором.
Адрес для приема заявок: test@vniiimt.ru


